 |
||||||

(Schulgerechter)
Nachweisgang ausgewählter organischer Substanzen:
Hinweise zu Schiffs Reagens
Mögliche Fehlerquellen:
| Selektivität: |
Die
Schiff'sche Probe eignet sich zur Unterscheidung der Alkanale von den
Kohlenhydraten. Nach Zugabe von Schiffs Reagenz tritt bei Alkanalen
sofort eine intensive
Rot-/Violett-Färbung auf. Das alles gilt aber offensichtlich nur, solange die Probe nicht erwärmt wird (siehe Prof. Blume, Link II, und Thomas Seilnacht, Link III). Regel:
Denn, wie leicht nachgeprüft werden kann:
Unter Wärmeeinwirkung zerfällt offenbar die (farblose) fuchsinschweflige Säure unter Freisetzung von Fuchsin (rot). Beim Abkühlen einer nicht zu stark - und nicht zu lang - erhitzten "Nicht-Aldehyd"-Probe mit Schiffs Reagenz sollte die aufgetretene Rotfärbung also wieder verschwinden (siehe Link IV, dort Nr. 8). Da durch die Wärmeeinwirkung die Konzentration der schwefligen Säure abnimmt (Freisetzung von Schwefeldioxid), bildet sich nach längerem bzw. starkem Erhitzen die fuchsinschweflige Säure allerdings auch in der Kälte nicht mehr zurück, die rote Farbe bleibt bestehen. Das Ausbleiben
der Farbreaktion mit Glucose - bei Zimmertemperatur! - lässt sich
auf eine zu geringe Konzentration "freier" Aldehyd-Gruppen
zurückführen. Die Regeneration des chromophoren Systems der
fuchsinschwefligen Säure durch Reaktion mit R-CHO ist dadurch nicht
mehr in ausreichendem Maße möglich. Diese Verringerung der
Aldehyd-Konzentration unter die Nachweisgrenze wird von Prof. Blume
(Link II) mit der im sauren Medium begünstigten Halbacetalbildung
der Glucose (Ringschluss) erklärt. Peter Keusch (Uni Regensburg;
Link V) und Prof. Seifert (Uni Bayreuth; Link VI) nennen eine weitere
mögliche Ursache: Das in Schiffs Reagenz enthaltene Hydrogensulfit-Ion
wird an die Aldehydgruppe der Probe addiert (Konkurrenzreaktion). "Der
Grund für das Ausbleiben der Schiff-Reaktion bei Glucose könnte in der
bevorzugten Bisulfitaddition bestehen" (Prof. Seifert, Link VI).
|
||
| Empfindlichkeit: | Da
die Schiffsche Probe sehr empfindlich ist, können bereits kleinste
Verunreinigungen zu Falsch-Positiv-Resultaten führen. Die verwendeten
Reagenzgläser, Pipetten und sonstigen Gerätschaften müssen
deshalb vor dem Versuch gründlich gereinigt werden; Blindproben
mit destilliertem Wasser oder Ethanol (siehe unten!) sind empfehlenswert.
Auch das bereitgestellte Schiffs Reagens selbst ist vor jeder
Verwendung auf eine evtl. bereits vorhandene Rotfärbung
zu überprüfen (aufgrund der Giftigkeit der schwefligen Säure
sollte die Zubereitung des Reagens nicht den SchülerInnen überlassen
werden). |
||
| Reihenfolge der Nachweise: | Unsachgemäße
Änderungen der Nachweis-Reihenfolge können - nicht nur in diesem
Fall - ebenfalls zu falschen Resultaten führen. So muss z. B. die
Fehling-Probe der Schiff'schen Probe vorangehen. Denn Alkohole
enthalten geringe Anteile ihrer Oxidationsprodukte, die bereits eine unklare
bzw. als positiv (fehl-)interpretierbare Schiff'sche Probe verursachen
können (siehe oben). Auch "Ethanol absolut zur Analyse, Gehalt
99,9%" - eine Qualität, die im Schulunterricht wohl eher selten
verwendet wird - 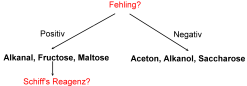 enthält
schon im Lieferzustand Spuren von Aldehyd. Eine vorhergehende Fehling-Probe
würde dagegen bereits an dieser Stelle - und mit größerer
Sicherheit - die Unterscheidung der Alkohole von den Alkanalen ermöglichen
und damit direkt zu den entsprechenden Nachweisschritten führen (Lukas-Probe,
Siedepunktbestimmung). enthält
schon im Lieferzustand Spuren von Aldehyd. Eine vorhergehende Fehling-Probe
würde dagegen bereits an dieser Stelle - und mit größerer
Sicherheit - die Unterscheidung der Alkohole von den Alkanalen ermöglichen
und damit direkt zu den entsprechenden Nachweisschritten führen (Lukas-Probe,
Siedepunktbestimmung). |
Links:
![]()